

RNA G-quadruplexes form scaffolds that promote neuropathological α-synuclein aggregation.
Kazuya Matsuo, Sefan Asamitsu, Kohei Maeda, Hiroyoshi Suzuki, Kosuke Kawakubo, Ginji Komiya, Kenta Kudo, Yusuke Sakai, Karin Hori, Susumu Ikenoshita, Shingo Usuki, Shiori Funahashi, Hideki Oizumi, Atsushi Takeda, Yasushi Kawata, Tomohiro Mizobata, Norifumi Shioda* and Yasushi Yabuki*
(* Co-corresponding authors)
Cell (in press) Oct 14:S0092-8674(24)01134-6.
doi: 10.1016/j.cell.2024.09.037
ポイント
概要説明
熊本大学発生医学研究所の塩田倫史教授、矢吹悌准教授および松尾和哉助教らの研究グループは、シヌクレイノパチーの発症機序を新たに解明しました。
シヌクレイノパチーは、パーキンソン病、レビー小体型認知症を含む進行性の神経変性疾患の総称です。シヌクレイノパチーでは、「αシヌクレイン」と呼ばれるタンパク質が細胞内に凝集することで神経機能の障害を引き起こしますが、その凝集機序は不明でした。本研究グループは、RNA高次構造のひとつである「グアニン四重鎖(G4)」の集積がαシヌクレイン凝集の足場となることを発見しました。パーキンソン病患者の剖検脳を解析したところ、αシヌクレイン凝集体の約90%にG4が集積していました。さらに、本研究グループが見出したG4の集積を抑制する薬剤である「5-アミノレブリン酸」(参考文献1)をシヌクレイノパチーモデルマウスに経口投与したところ、αシヌクレインの凝集が阻害され、進行性の運動機能の低下が予防できました。
これまで本研究グループは、遺伝性の神経変性疾患においてもG4の集積が神経機能の障害を引き起こすことを報告しています(参考文献2)。また、アルツハイマー病に深く関わる「タウ」と呼ばれるタンパク質もG4により凝集することも明らかにしています(参考文献3)。すなわち、「G4の集積」を抑制することは、神経変性疾患全般の「未病」に向けた創薬に繋がります。
本研究成果は、文部科学省科学研究費助成事業(課題番号:JP21K20723, JP22J00687, JP21K06579, JP23H03851, JP21H00207, JP20K21400, JP22K19297, JP23H00373)、日本医療研究開発機構(AMED)革新的先端研究開発支援事業「RNA相転移によるプリオン性タンパク質のプロテオスタシス破綻機構」(課題番号:JP23gm6410021h0003)、脳とこころの研究推進プログラム「RNA相転移によるシヌクレイノパチー発症機序の解明」(課題番号:JP23wm0525023h0003)、JST創発的研究支援事業「グアニン四重鎖によるプリオノイド・イノベーション」(JPMJFR2043)、熊本大学発生医学研究所共同研究拠点、熊本大学発生医学研究所高深度オミクス医学研究拠点ネットワーク形成事業、文部科学省共同利用・共同研究システム形成事業「学際領域展開ハブ形成プログラム」などの支援を受けて、科学雑誌「セル(Cell)」オンライン版に米国(ET)時間の令和6年10月18日午前11時(日本時間10月19日午前0時)に掲載されました。
説明
[背景]
社会の高齢化に伴い神経変性疾患の患者は急速に増加しており、その対策は喫緊の課題となっています。シヌクレイノパチー(パーキンソン病、レビー小体型認知症、多系統萎縮症など)やタウオパチー(アルツハイマー病など)は、脳内に異常なタンパク質が凝集・蓄積・細胞間伝播することで神経細胞の機能低下を引き起こし、認知障害や運動障害などの症状を呈します。
シヌクレイノパチーでは、「αシヌクレイン」と呼ばれるタンパク質が細胞内に凝集し、神経障害を引き起こします。しかしながら、「通常は凝集しないαシヌクレインが、どのように細胞内で凝集するのか」は未解明でした。
[研究の内容]
本研究グループは、αシヌクレインを細胞内で凝集する分子の同定に成功しました。それは、「G4」と呼ばれるRNA高次構造でした。G4は、細胞にストレスが付加されると増加・集積しますが(参考文献4)、「G4の集積」はαシヌクレインを凝集させる足場となることがわかりました。実際、パーキンソン病患者の剖検脳において、αシヌクレイン凝集体の約90%にG4が集積していました。また、G4を人為的にマウス脳内の神経細胞に集積させたところ、細胞内のαシヌクレインがG4の集積を足場として凝集し、神経変性と運動機能障害を引き起こしました。さらに、本研究グループが見出したG4の集積を抑制する薬剤である「5-アミノレブリン酸」(参考文献1)をシヌクレイノパチーモデルマウスに経口投与したところ、αシヌクレインの凝集が阻害され、進行性の運動機能の低下が予防できました。
[成果・展開]
今回、αシヌクレインを細胞内で凝集する分子が「G4」であることを初めて同定し、「G4の集積抑制」によってシヌクレイノパチーの発症を予防できることを証明しました。これまで本研究グループは、遺伝性の神経変性疾患においてもG4の集積が神経変性を引き起こすことを報告しています(参考文献2)。また、アルツハイマー病に深く関わる「タウ」と呼ばれるタンパク質もG4により凝集することも明らかにしています(参考文献3)。すなわち、「G4の集積」を抑制することは、神経変性疾患全般の「未病」に向けた創薬に繋がります。
[用語解説]
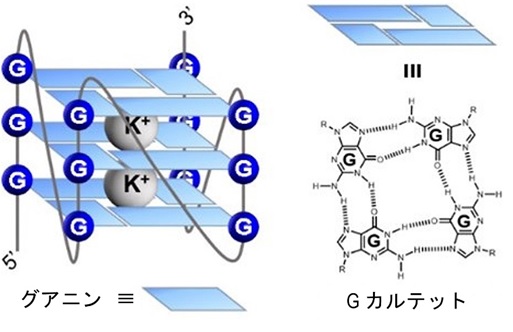
*グアニン四重鎖(G4): DNAおよびRNAの高次構造の一種。グアニンに富む核酸配列で形成される。4つのグアニンが四量体を作った面(G-カルテット)が2面以上重なった構造体である(下図)。本研究では、RNAで形成されるG4の集積がαシヌクレイン凝集の足場となることを示した
参考文献1:Shioda et al. Nature Medicine 24, 802-813. (2018)
参考文献2:Asamitsu et al. Science Advances 7, eabd9440. (2021)
参考文献3:Yabuki et al. bioRχiv doi: https://doi.org/10.1101/2024.03.01.582861
参考文献4:Asamitsu et al. Science Advances 9, eade2035. (2023)
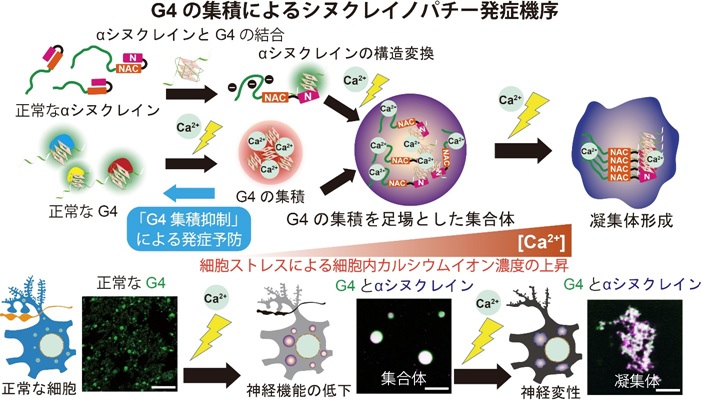
[図説]
神経変性の引き金となるのは、細胞ストレスによる細胞内カルシウムイオン(Ca2+)の濃度上昇に伴うG4の集積である。さらに、αシヌクレインはG4と直接結合し凝集性のある形状に構造変換する。G4の集積を足場とし、αシヌクレインが凝集体を形成する。したがって、G4の集積を抑制することはαシヌクレインの凝集抑制に繋がり、神経機能の低下を予防できる。
Targeting G-quadruplex DNA as cognitive function therapy for ATR-X syndrome.
Norifumi Shioda, Yasushi Yabuki, Kouya Yamaguchi, Misaki Onozato, Yue Li, Kenji Kurosawa, Hideyuki Tanabe, Nobuhiko Okamoto, Takumi Era, Hiroshi Sugiyama, Takahito Wada, Kohji Fukunaga. Nature Medicine 24, 802-813. (2018)
私達は、ATR-X 症候群でみられる知的障がいに有効な治療薬の探索を行いました。その結果、既に市場で安全性に関する情報が整備されている既存薬である「5-アミノレブリン酸」が今まで知られていない薬理作用によりATR-X 症候群モデルマウスの知的障がいに有効であることを発見しました。
私たちの遺伝情報(ヒトゲノム)を司るDNAには、繰り返し配列により「グアニン四重鎖」と呼ばれる特殊な DNA 構造をとる場所が多数存在します。この構造は遺伝子の働きに重要と考えられています。ATRXタンパク質はこの「グアニン四重鎖」に結合し、遺伝子が正常に働くように調節します。5-アミノレブリン酸を服用すると、体内でグアニン四重鎖に作用する物質であるポルフィリンが産生され、 ATRXタンパク質の機能を補うことができることがわかりました。グアニン四重鎖はその他の難治性疾患の病態にも関与しており、今回の発見は新しい創薬標的発見の可能性に寄与することが期待できます。
1.背景
ATR-X 症候群 (X連鎖αサラセミア知的障がい症候群) 注1はX 染色体上の責任遺伝子である ATRX の変異により男性のみで発症するX連鎖知的障がい症候群の一つです。主症状として重度の知的障がいが挙げられますが、いまだ治療薬がなく詳しい発症機構も明らかにされていません。日本国内では約 100 症例が診断されており、世界では日本の症例を含め 200 症例以上が診断されています。 ATR-X症候群では ATRX 遺伝子の変異により、ATRX タンパク質が機能していないことが報告されています。また、 ATRX タンパク質は核内クロマチンリモデリング因子 注2 であり、特殊な DNA の構造体であるグアニン四重鎖 注3に結合することで遺伝子の発現を調節することが知られています。しかしながら、なぜ核内で機能する因子である ATRX タンパク質の機能低下が知的障がいの原因になるのか不明でした。本研究グループは、ATR-X 症候群における知的障がいの病態をATR-X 症候群モデルマウスを用いて解析しました。そして、ATR-X 症候群の知的障がいに有効な薬剤の探索を試みました。
2.研究成果
1)ATR-X 症候群における知的障がいの分子機構を解明
本研究グループは、学習・記憶に重要な役割を担う脳の海馬領域でATR-X 症候群モデルマウスを用いて網羅的な遺伝子発現解析を行いました。その結果、X染色体上の母由来インプリント遺伝子注4である Xlr3b が脳特異的に異常に発現が上昇していることを発見しました。本研究グループは、ATRX タンパク質が Xlr3b 遺伝子上流のグアニン四重鎖に結合し、 Xlr3b の DNA メチル化注5を制御することで、Xlr3b の発現を調節していることを明らかにしました。また、Xlr3b の異常な発現上昇が神経細胞の樹状突起 mRNA 輸送注6を抑制することで ATR-X 症候群モデルマウスの神経機能を低下させることを発見しました。
2)ATR-X 症候群における知的障がいに有効な薬剤を発見
ATRX タンパク質はグアニン四重鎖に結合し、遺伝子発現を調節することから、グアニン四重鎖が治療標的のひとつとして考えられます。これまで、グアニン四重鎖に結合する物質とてポルフィリン骨格を有する化合物がいくつか知られています。本研究グループは、生体内でポルフィリンを産生することができる安全性の高い薬剤「5-アミノレブリン酸」を ATR-X 症候群モデルマウスに投与し、認知機能に対する薬効評価を行いました。生後 、離乳してから2ヶ月間、長期的に口から飲ませたところ、ATR-X 症候群モデルマウスでみられた認知機能障がいが改善しました。さらに、網羅的遺伝子発現解析の結果、ATR-X 症候群モデルマウス脳において発現異常がみられた遺伝子の約70% を改善することができ、その中に Xlr3b も含まれていました。
3.波及効果、今後の予定
本研究では、ATR-X 症候群における知的障がいの分子機構にグアニン四重鎖が関与することを発見し、薬剤「5-アミノレブリン酸」が認知機能障がいの改善に有効であることを確認しました。難治性疾患「ATR-X症候群」の治療に新たな光を投げかける画期的な成果といえます。また、グアニン四重鎖は近年、 C9ORF72 遺伝子のもつ GGGGCC リピート配列の異常伸長による家族性の筋萎縮性側索硬化症(ALS)注7等、様々な難治性神経疾患の病態においても注目されています。今回の発見は、こうした難病の新しい創薬標的の可能性にも寄与することが期待できます。
<用語解説>
Endocytosis following dopamine D2 receptor activation is critical for neuronal activity and dendritic spine formation via Rabex-5/PDGFRβ signaling in striatopallidal medium spiny neurons.
Norifumi Shioda, Yasushi Yabuki, Yanyan Wang, Motokazu Uchigashima, Takatoshi Hikida, Toshikuni Sasaoka, Hisashi Mori, Masahiko Watanabe, Masakiyo Sasahara and Kohji Fukunaga Molecular Psychiatry 22,1205-1222. (2017)
1.背景
私達は細胞内ドパミンD2受容体の新たな生理機能を発見しました。ドパミンは感情・意欲・運動・学習などに関わる重要な神経伝達物質です。ドパミン受容体の中で細胞膜D2受容体は統合失調症や注意欠陥多動性障害の治療薬の標的であり、ドパミンの中枢作用を担っていると考えられています。本研究では細胞内D2受容体の活性化機構とシナプス機能を明らかにしました。
ドパミン受容体は7回膜貫通型のG蛋白質共役型受容体です。ヒトゲノム解析からドパミンD2受容体には統合失調症・パーキンソン病・薬物依存の患者に共通する遺伝子多型が見出されています。しかし、 細胞内ドパミンD2受容体と精神・運動との関わりは不明でした。また、ドパミンD2受容体にはD2L受容体とD2S受容体の2種類の構造の異なる受容体が存在しますが、D2L受容体とD2S受容体の機能的役割の違いは不明です。本研究では、D2L受容体の新しい細胞内シグナル伝達機構を発見し、そのシナプス機能を解明しました。即ち、D2L受容体は細胞膜表面に加えて、細胞内小器官(初期エンドソームとゴルジ装置)に局在し、抗精神病薬による精神安定作用と錐体外路系機能制御に関与することを証明しました。
2.研究成果
Rabex-5 は初期エンドソームの形成に関与する低分子量G蛋白質Rab5の活性化因子です。ドパミンが細胞膜D2L受容体に作用するとD2L受容体とRabex-5、Rab5及び血小板由来増殖因子(PDGF)受容体は初期エンドソームに集積します。ダイナミン依存性のエンドサイトーシスにより細胞内に取り込まれ、初期エンドソーム・ゴルジ装置に局在する細胞内D2L受容体と複合体を形成することで、神経活動とそれに伴った運動機能を制御します。本研究成果は細胞内ドパミン受容体の生理機能を実証した初めての成果であり、細胞内D2L受容体が新しい錐体外路機能調節薬及び精神疾患治療薬の新しい創薬標的であることを示しました。
3.波及効果、今後の予定
細胞内D2L受容体と血小板由来増殖因子(PDGF)受容体の協同による活性化機構は、運動機能よりも精神機能改善に深く関与すると考えられます。実際に細胞内D2L受容体を活性化することで精神疾患治療薬に対する感受性が改善します。本発見により細胞内D2L受容体及び PDGF 受容体の協力作用を目指した精神疾患の新規治療薬の開発が期待できます。