論文名
FOXF1/2 establish senescence-specific enhancer landscape to activate pro-inflammatory senescence-associated secretory phenotype(FOXF1/2が老化細胞に特徴的な炎症性エンハンサーを確立して、細胞老化関連性分泌表現型を活性化する)
著者名(*責任著者)
Kan Etoh*, Yuko Hino, Hideaki Morishita, and Mitsuyoshi Nakao*
掲載雑誌
Molecular Cell
https://www.cell.com/molecular-cell/fulltext/S1097-2765(26)00196-6
ポイント
概要説明
熊本大学発生医学研究所 細胞医学分野 の 衛藤 貫 特任助教(現 九州大学医学研究院・助教)、中尾 光善 特任教授らは、網羅的な遺伝子・ゲノム解析を用いて、老化細胞*1による慢性炎症*2を促進する主要な転写因子「FOXF1/2」*3を初めて発見しました。転写因子はゲノム上の標的遺伝子の働きを選択的に促進したり、抑制したりすることができます。転写因子が働く場をクロマチン*4と呼んで、働かない遺伝子ではこの構造が閉鎖しており(OFFの状態)、他方、働く遺伝子ではオープンな構造にあります(ONの状態)。OFFからONへの変換を最初に担う転写因子を「パイオニア転写因子」と呼びます。今回、老化細胞において、FOXF1/2が炎症性タンパク質の遺伝子のエンハンサー領域*5に集結して働くことが分かりました。FOXF1/2は炎症性タンパク質の遺伝子のエンハンサーでヒストンのアセチル化*6を促進し、閉じたOFFの状態からオープンなONの状態になることで、これらの遺伝子が活性化します。また、AP-1(c-JUN)*7と共同して、パイオニア転写因子として働くことを明らかにしました。老化細胞でFOXF1/2またはc-JUNを阻害したところ、炎症性タンパク質の遺伝子が強く抑制されて、炎症反応が低下することを見出しました。
この成果では、老化細胞でFOXF1/2が炎症性タンパク質の合成・分泌を促進するメカニズムを明らかにしたことから、細胞老化による慢性炎症の制御法(セノスタティクス*8)の開発につながることが期待されます。
本研究成果は、文部科学省科学研究費補助金、文部科学省共同利用・共同研究システム形成事業「学際領域展開ハブ形成プログラム」、熊本大学発生医学研究所の高深度オミクス医学研究拠点ネットワーク形成事業、熊本大学わかば研究推進事業、金原一郎記念医学医療振興財団助成金などの支援を受けて、科学雑誌「モリキュラー・セル(Molecular Cell)」オンライン版に米国(ET)時間の令和8年4月16日11:00【日本時間の4月17日(金)0:00】に掲載されました。
用語解説
*1:老化細胞:増殖を持続的に停止した状態の細胞を老化細胞という。加齢と共に体内に生存・蓄積して予想以上に活発な活動を行う。
*2:慢性炎症:比較的に弱い程度で長期に渡って炎症反応がある状態を慢性炎症という。加齢・老化に伴うことが多く、組織や器官の機能低下につながる。
*3:転写因子「FOXF1/2」:細胞内で標的の遺伝子の働きを調節するタンパク質を転写因子と呼ぶ。その中で、FOXF1/2の機能はよく分かっていなかった。パイオニア転写因子が標的遺伝子を開いた後に、他の転写因子が作用できる。
*4:クロマチン:ゲノムDNAとヒストンなどのタンパク質の複合体。閉じたクロマチンの構造にある遺伝子は働かず、他方、オープンなクロマチンの構造にある遺伝子は働きやすくなる。
*5:エンハンサー領域:ゲノム上の遺伝子の働きを促進する特徴的なDNA配列。特定の転写因子(DNA結合タンパク質)が結合して調節される。
*6:ヒストンのアセチル化:アセチルCoAを用いてアセチル基転移酵素がヒストンタンパク質を修飾する。その結果、オープンなクロマチンの構造をおこす。
*7:AP-1(c-JUN):AP-1は代表的な転写因子のタンパク質複合体であり、これを構成する主なタンパク質がc-JUNで、遺伝子の働きを調節する。
*8:セノスタティクス:老化細胞を保持して炎症反応を選択的に制御する方法。近年、薬剤によるセノリティクス(老化細胞除去)が注目されるが、老化細胞を除去すると組織の線維化が生じるという報告がある。セノ(老化)+リティクス(分解)、スタティクス(静力学)の造語。
研究の内容及び成果
我が国の高齢化は、世界に類を見ないスピードで進展し、今後も平均寿命が続くと予想されることから、“健康を維持しながら老いる”健康寿命が重要になっています。身体を構成する多くの細胞は、分裂を繰り返して増えると、やがてその細胞自体の機能は低下して増殖を停止します。これを「細胞老化」とよんで、全身の老化と慢性炎症に関わる重要な要素と考えられています【図1】。細胞老化は、放射線や紫外線などの物理的なストレス、食事や薬剤などの化学的なストレスによってゲノムDNAが損傷を受けると促進されることが知られていますが、老化細胞のメカニズムはよく分かっていません。しかも、細胞老化には良い点も悪い点もあります。細胞が「がん化」を始めると、細胞老化が生じてがんの発生を防ぐ役割をしています。他方、細胞老化によって多くの病気(認知症、糖尿病、動脈硬化など)が起こりやすくなります。したがって、細胞老化は適切に制御されることが重要です。
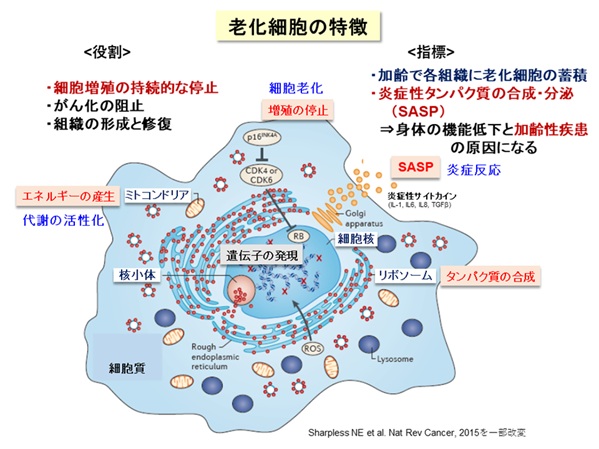
図1
「老化細胞」は増殖能を失いますが、近年、老化細胞がさまざまな炎症性タンパク質(サイトカイン、ケモカインとよばれます)を分泌して周囲の細胞に働きかけて、慢性的な炎症やがん細胞の増殖を促進することが注目されています【図1】。この特徴は「細胞老化関連性分泌表現型(SASP)」とよばれています。このように、老化細胞はアクティブに働いているので、細胞老化は、身体全体の老化の原因になると考えられるわけです。例えば、老齢マウスの体内には老化細胞が蓄積していきますが、これらを除去すると全身の老化が抑えられて改善するという報告があります。このため、薬剤による「セノリティクス」(老化細胞除去)が注目されています【図2】。ところが、体の中で老化細胞は一定の役割を果たしていて、老化細胞が除去されると、その隙間を埋めるように組織の線維化が進んで機能低下するという報告もあるため、世界中でさまざまな研究が進行中にあります。つまり、細胞老化とSASPを制御できれば、全身の老化の進度を調節できる可能性があります。
本研究グループは、「エピジェネティクス」とよばれる学問の観点から、細胞老化のメカニズムについて研究を進めています。エピジェネティクスは、すべての遺伝子の働き方(ON/OFF)を明らかにする研究分野であり、生命現象や病気の発症、さらに老化にも密接に関わると考えられます【図3】。ヒトの設計図に当たるゲノムには、約2万個の遺伝子(タンパク質をつくる)があります。我々はヒト線維芽細胞(すべての組織・器官に存在する細胞種)の老化に関わる因子を幅広くスクリーニングして、鍵となる複数の因子を同定してきました。現在までに、老化細胞では「RBがん抑制タンパク質」によってミトコンドリアの代謝機能が著しく上昇していること(2015年)、「SETD8メチル基転移酵素」および「NSD2メチル基転移酵素」などが細胞老化を防ぐ役割をもつこと(2017年、2020年)を報告しました。さらに、老化細胞では、炎症性タンパク質の遺伝子群に位置するヒストンが「ACLY」(クエン酸からアセチルCoAを合成する酵素)由来のアセチルCoAを用いてアセチル化されること、ACLY阻害剤を用いて、炎症性SASPを選択的に阻害できること(セノスタティクス)を報告しました(2024年)。
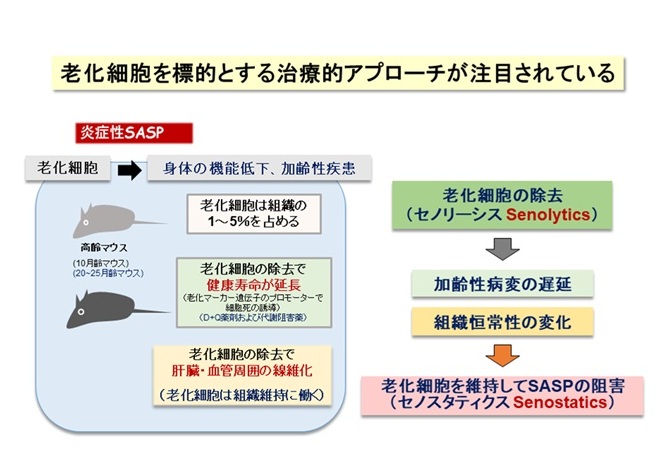
図2
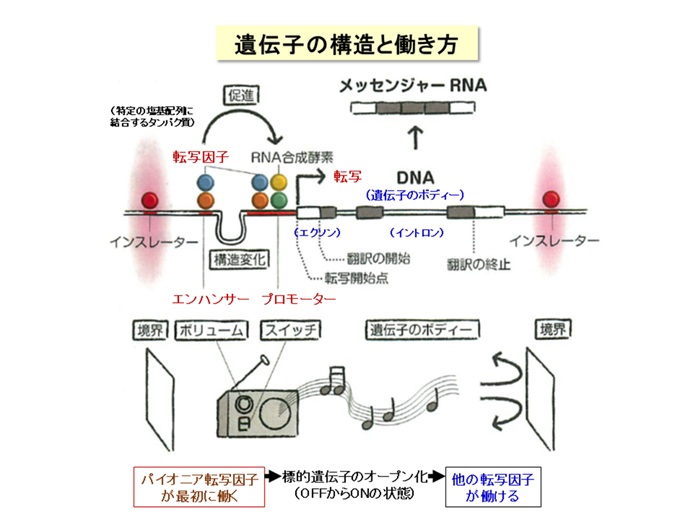
図3
正常な細胞は、何度も分裂して複製した後に増殖を停止します(複製後の細胞老化)。また、がん遺伝子が活性化してがん化が始まると、それを阻止するために老化がおこります(がん遺伝子で誘導される細胞老化)。この老化細胞について、最新のシークエンサーを用いたバイオ情報解析を行って、老化細胞の全遺伝子発現を網羅的に調べる中で、「FOXF1/2」が炎症性タンパク質(SASP)遺伝子群のパイオニア転写因子として働くことを見出しました【図4】。ゲノムDNAに巻き付く「ヒストン」タンパク質がアセチル化されて、その近傍の遺伝子の働きを促すことが知られています。これまでの「ACLY」の研究成果から、炎症性SASP遺伝子の働きはヒストンのアセチル化を介して促進されることに着目しました。しかし、「ヒストンアセチル基転移酵素」(p300/CBPとよぶ)がどのように炎症性SASP遺伝子群を標的にするのか、遺伝子の選択性のメカニズムは分かっていません。そこで、老化した線維芽細胞において、p300/CBPの働きを抑えるノックダウン(RNA干渉法)を行ったところ、数多くの炎症性SASP遺伝子群のエンハンサーが閉じて、その遺伝子群の働きが抑制されることが分かりました。注目すべきことに、細胞老化の状態を保ちながら、炎症性SASPが選択的に阻止されました。炎症性SASP遺伝子群で閉じたエンハンサー領域には、「FOXF1/2」の結合配列が集積しており、本来の老化細胞ではFOXF1/2が集結することが分かりました。さらに、FOXF1/2を阻害するノックダウンを用いると、同様に炎症性SASP遺伝子領域が閉じて、SASPと炎症反応が抑制されることを確認しました。つまり、FOXF1/2阻害で老化細胞の炎症性SASPが阻止されることが明らかになりました【図5】。
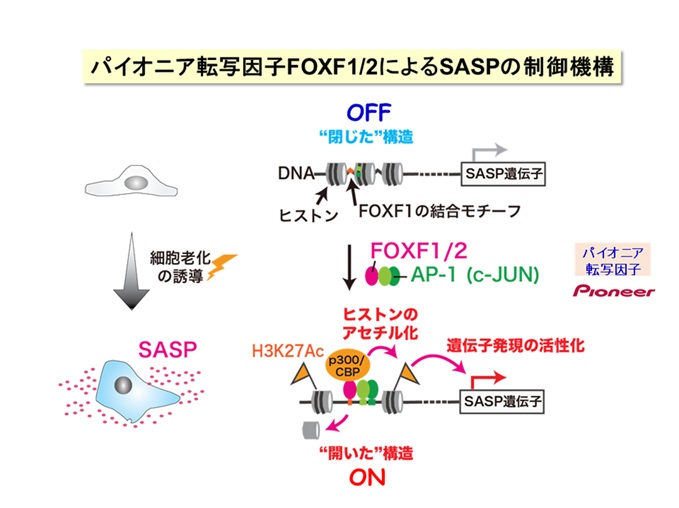
図4
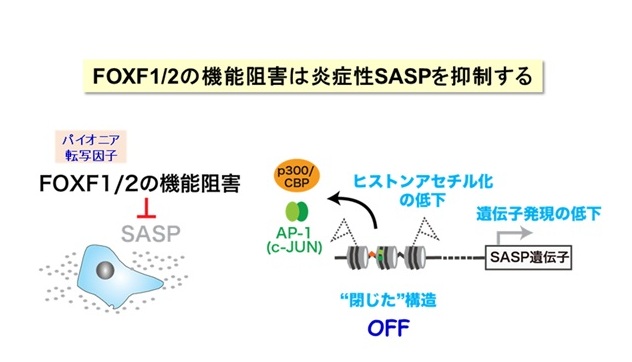
図5
次に、老化細胞におけるFOXF1/2の役割を詳しく調べた結果、①FOXF1/2ともうひとつの転写因子AP-1(c-JUN)が共同して、炎症性SASP遺伝子群のパイオニア転写因子として働くこと、②炎症性SASP遺伝子群に作用する場合、FOXF1/2とAP-1(c-JUN)がお互いに必要であること、③FOXF1/2阻害またはc-JUN阻害を用いて、老化細胞の炎症反応が抑制できること、が分かりました。すなわち、老化細胞では、炎症性SASP遺伝子群のエンハンサー領域にFOXF1/2とAP-1(c-JUN)が作用して、ヒストンがアセチル化されて、その部分がオープンな構造になって、これらの遺伝子群の働きが促進されるわけです。このため、FOXF1/2とc-JUNによる細胞老化プログラムを制御すれば、炎症性SASPと慢性炎症を選択的に抑制できること(セノスタティクス)が明らかになりました【図6】。
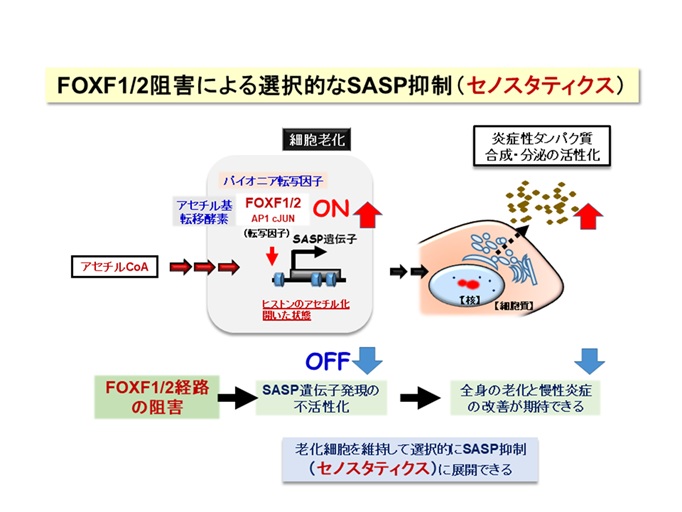
図6
今回の研究成果は、細胞老化の炎症性SASPを確立・維持するパイオニア転写因子FOXF1/2を発見したことを契機として、細胞老化の基本メカニズムを明らかにしたものです。FOXF1/2の働きを調節すれば、老化細胞を維持したまま、慢性炎症を引き起こす炎症性SASP遺伝子群を最も根本的に制御する手法の開発に役立つと期待できます。
概要ポイントの専門的な補足説明 【図6】
1) 炎症性SASP遺伝子群は、アセチル基転移酵素p300/CBPを介したヒストンのアセチル化によって活性化されます。p300/CBPの働きを阻害すると、アセチル化の減少とエンハンサーの閉鎖によってこれらの遺伝子が抑制されます。
2) パイオニア転写因子FOXF1/2は、炎症性SASP遺伝子群におけるエンハンサーの働きを先導します。老化細胞の主要なFOX転写因子であるFOXF1/2は、細胞の増殖停止とは独立して、炎症性SASP遺伝子群の働きを促進します。
3) FOXF1/2は、p300/CBPを介して炎症性SASP遺伝子群のアセチル化とオープン化を誘導します。FOXF1/2の働きを阻害すると、エンハンサーにおけるアセチル化の減少とその閉鎖によって、この遺伝子の働きが抑制されます。
4) FOXF1/2はもうひとつの転写因子AP-1(c-JUN)と共同して炎症性SASP遺伝子群のエンハンサーに作用します。この作用に両者が互いに必要であり、FOXF1/2またはAP-1(c-JUN)を阻害すると、遺伝子の働きが抑制されます。
5) FOXF1/2を介した炎症性SASPプログラムが明らかになり、老化細胞を維持しながらSASPを選択的に制御することから、健康的な老化を促進するためのセノスタティックス(老化抑制薬)の重要な標的であると期待されます。